Автор:
Lewis Jackson
Жасалған Күн:
12 Мамыр 2021
Жаңарту Күні:
1 Шілде 2024

Мазмұны
Атомдағы нейтрондардың санын анықтау өте қарапайым, тіпті тәжірибе жасаудың қажеті жоқ. Қалыпты атомдағы немесе изотоптағы нейтрондар санын есептеу үшін тек периодтық кесте дайын болып, нұсқауларды орындау керек.
Қадамдар
2-ден 1-әдіс: Қалыпты атомдағы нейтрондардың санын табыңыз
Периодтық жүйедегі элементтің орнын анықтаңыз. Мысалы, біз осмий (Os) элементін алтыншы қатардан жоғарыдан табамыз.
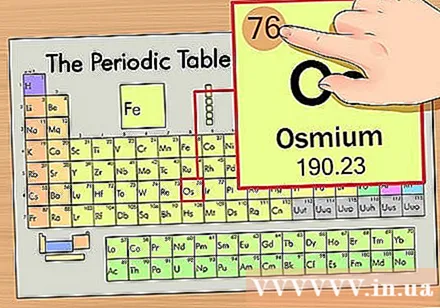
Элементтің атомдық нөмірін табыңыз. Бұл әр элемент бойынша жүретін және жай символдан жоғары орналасқан ең айқын сан (біз қолданып отырған тақтада басқа сандар жоқ). Атомдық сан - бұл осы элементтің бір атомындағы протондар саны. Os - бұл 76 саны, яғни осмий атомында 76 протон бар.- Протондардың саны элементте ешқашан өзгермейді; ол мәні бойынша элементтің анықтаушы сипаттамасы болып табылады.
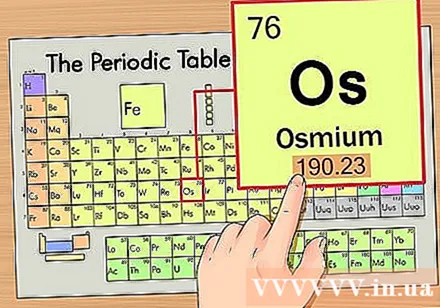
Элементтің атомдық салмағын табыңыз. Бұл сан, әдетте, қарапайым белгінің астында орналасады. Осы мысалдағы периодтық жүйеде тек атомдық нөмір бар және атомдық салмақ жоқ екенін ескеріңіз. Барлық периодтық кестелер емес. Осмийдің атомдық салмағы 190,23 құрайды.
Атом массасын алу үшін атом салмағын бүтін санға дейін дөңгелектеңіз. Мысалы, 190.23 190-ға дейін дөңгелектенеді, сондықтан осмийдің атомдық массасы 190-ға тең.- Атомдық салмақ - бірдей химиялық элементтің изотоптарының орташа мәні, сондықтан ол әдетте бүтін сан болмайды.
Атомдық саннан атомдық санды алып тастаңыз. Атомдық массаның көп бөлігі протондар мен нейтрондардың массасы болғандықтан, атом массасынан протондар санын алып тастағанда (яғни, атомдық санда) санау атомдағы нейтрондардың санын алу. Ондық нүктеден кейінгі сан атомдағы электрондардың өте аз массасын білдіреді. Бұл мысалда бізде: 190 (масса атомы) - 76 (протондар саны) = 114 (нейтрондар саны).
Рецептті жаттап алыңыз. Нейтрондардың санын табу үшін біз келесі формуланы қолданамыз: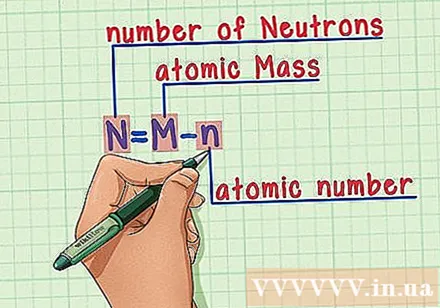
- N = M - n
- N = нейтрондар саны
- M = атомдық масса
- n = атом саны
- N = M - n
2-ден 2-әдіс: Изотоптағы нейтрондардың санын табыңыз
Периодтық жүйедегі элементтің орнын анықтаңыз. Мысал ретінде көміртек-14 элементтік изотопын алайық. Көміртектің-14 изотоптық формасы жай көміртегі болғандықтан, көміртекті периодтық жүйеден іздеңіз (жоғарыдан екінші қатар).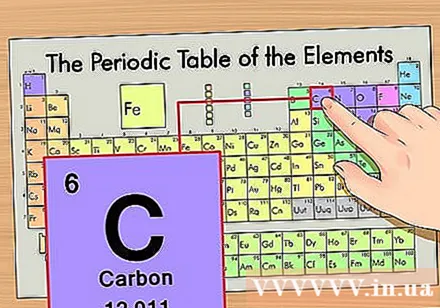
Элементтің атомдық нөмірін табыңыз. Бұл әр элемент бойынша жүретін және жай символдан жоғары орналасқан ең айқын сан (біз қолданып отырған тақтада басқа сандар жоқ). Атомдық сан - бұл осы элементтің бір атомындағы протондар саны. C - бұл 6 саны, яғни көміртек атомында 6 протон бар.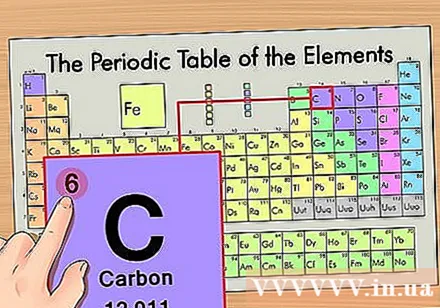
Атомдық массаны табыңыз. Бұл изотоптармен өте оңай, өйткені олар атомдық массаға байланысты. Мысалы, көміртек-14 атомдық массасы 14-ке тең болар еді. Изотоптың атомдық массасын тапқаннан кейін нейтрондар санын табудың қалған қадамдары қалыпты атоммен бірдей болады.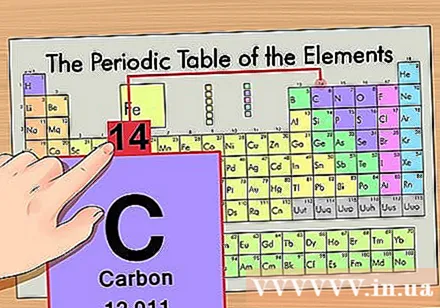
Атомдық саннан атомдық санды алып тастаңыз. Атомдық массаның көп бөлігі протондар мен нейтрондардың массасы болғандықтан, атом массасынан протондар санын алып тастағанда (яғни, атомдық санда) санау атомдағы нейтрондардың санын алу. Ондық нүктеден кейінгі сан атомдағы электрондардың өте аз массасын білдіреді. Бұл мысалда бізде: 14 (масса атомы) - 6 (протондар саны) = 8 (нейтрондар саны) бар.
Рецептті жаттап алыңыз. Нейтрондардың санын табу үшін келесі формуланы қолданамыз: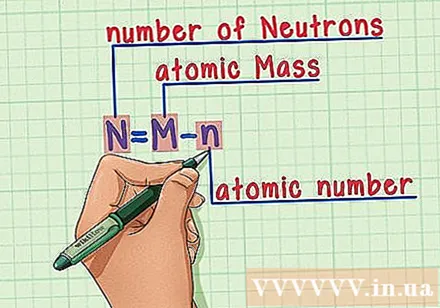
- N = M - n
- N = нейтрондар саны
- M = атомдық масса
- n = атом саны
- N = M - n
Кеңес
- Элементтің массасы көбінесе протондар мен нейтрондардың массаларын құрайды, ал электрондар мен басқа элементтердің массалары шамалы (нөлге жақын). Протонның массасы шамамен нейтронның массасына тең болғандықтан және атом саны протондар санын білдіреді, біз жай протондар санын жалпы массадан алып тастаймыз.
- Егер сіз периодтық жүйедегі сандардың мағынасын есіңізде сақтамасаңыз, онда периодтық жүйе көбінесе атомдық сандарға (яғни протондар саны) 1-ден (сутектен) басталып, бір бірліктен бастап көбейетіндігін ескеріңіз. солдан оңға қарай 118-мен аяқталады (унуноций). Протондардың саны әр атомның идентификациялық ерекшелігі болғандықтан, бұл элементтер орналасқан қарапайым қасиет. (Мысалы, 2 протонды атом әрдайым гелий болады, 79 протонды атом әрдайым алтын болады).
Дереккөздер мен дәйексөздер
- Интерактивті периодтық кесте