Автор:
Lewis Jackson
Жасалған Күн:
6 Мамыр 2021
Жаңарту Күні:
1 Шілде 2024
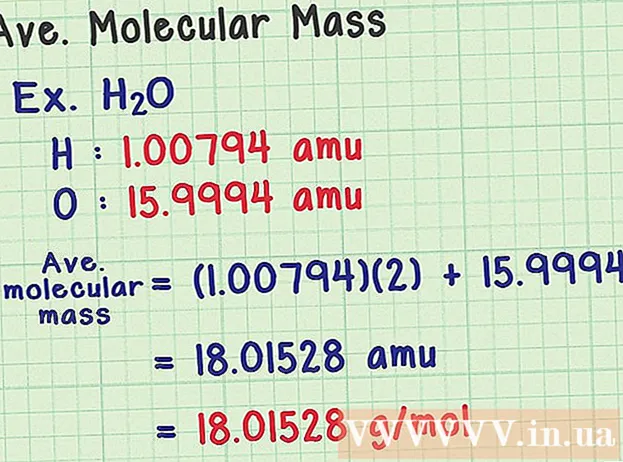
Мазмұны
Орташа атом атомы массасының тікелей өлшемі емес. Оның орнына, бұл элементтің әдеттегі үлгісінен бір атомға келетін орташа масса. Егер сіз миллиардтаған жеке атомдардың массасын өлшей алсаңыз, мұны олардың орташа мәндерін есептеу арқылы білуге болады. Бізде химиялық элементтің әртүрлі изотоптары туралы ақпаратқа негізделген практикалық әдіс бар.
Қадамдар
2-ден 1-бөлім: орташа масса атомын есептеңіз
Изотоптар мен массалық атомдарды түсіну. Табиғатта көптеген элементтер әртүрлі формада немесе изотоптарда болады. Бір элементтің екі изотоптарының арасындағы айырмашылық тек атомдағы нейтрондардың саны, олардың нейтрондар саны массалық атомға әсер етеді. Орташа массалық атомды есептеу осы айырмашылықтың әсерін ескереді және сол атомдардың үлгісіндегі әр атомның орташа массасын айтады.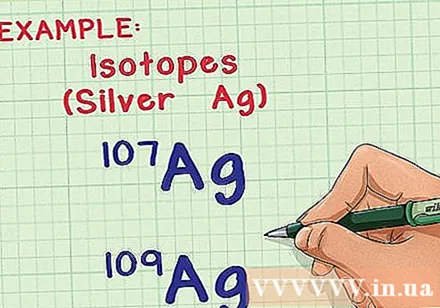
- Мысалы, күміс (Ag) элементінің екі табиғи изотоптары бар: Ag-107 және Ag-109 (немесе Ag және Ag). Изотоп «массалық санның» немесе протондар мен атомдағы нейтрондар санының қосындысымен аталады. Демек, Ag-109-да Ag-107-ге қарағанда екі нейтрон көп, сондықтан оның атомы біршама ауыр.
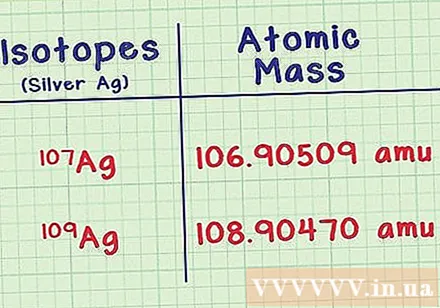
Әр изотоптың массасын табыңыз. Сізге әр изотоп үшін екі ақпарат қажет, оларды анықтамалық кітаптардан немесе интернеттен іздеуге болады, мысалы webelements.com. Біріншісі - әрбір изотоптың массалық атомы немесе атомдық массасы. Нейтрондары көп изотоптардың массасы көп.- Мысалы, күміс изотоп Аг-107 массалық атомға ие 106,90509 аму (куб атомының бірлігі). Ag-109 изотопы массасынан сәл ауыр 108,90470.
- Соңындағы ондықтар жұбы құжаттарда сәл өзгеше болуы мүмкін. Массадан кейін жақшаға ешқандай сандар жазуға болмайды.

Әр изотоп үшін табиғи тіршілік ету коэффициентін жазыңыз. Бұл коэффициент изотоптың кең таралуын көрсетеді, бұл элементтің жалпы атомдарының пайызына тең. Бұл ақпаратты сіз текшелік атомы бар бір құжаттан таба аласыз. Барлық изотоптардың табиғи өмір сүруі 100% құрауы керек (бірақ дөңгелектеу қателігінен ол аздап ерекшеленуі мүмкін).- Аг-107 изотопының қатынасы 51,86% құрайды. Аг-109 изотопы 48,14% жылдамдығымен аз таралған. Демек, қалыпты күмісте 51,86% Ag-107 және 48,14% Ag-109 болады.
- Мұндай тіршілік ету жылдамдығы жоқ кез-келген изотоптар еленбейді. Бұл изотоптар жер бетінде табиғи түрде жоқ.

Изотоп пайызын ондық санға ауыстырыңыз. Бұл қатынасты 100-ге бөлгенде, ондық санмен бірдей мән шығады.- Жоғарыдағы күміс сынамада изотоптардың қатынасы 51,86 / 100 = құрайды 0,5186 және 48,14 / 100 = 0,4814.
Орташа кубтық атомды табыңыз. Элементтің орташа массалық атомы бар n изотоптар тең (Атом блогыИзотоп 1 * арақатынасИзотоп 1) + (атомдық массаИзотоп 2 * арақатынасИзотоп 2) + ... + (атомдық масса)изотоптар n * арақатынасизотоптар n. Бұл «орташа массаның» мысалы, яғни изотоптың тіршілік ету коэффициенті неғұрлым көп болса, оның нәтижеге әсері соғұрлым жоғары болады. Бұл формуланы күміске қалай қолдануға болады:
- Орташа атомАг = (куб атомыАг-107 * арақатынасАг-107) + (атомдық массаАг-109 * арақатынасАг-109)
=(106,90509 * 0,5186) + (108,90470 * 0,4814)
= 55,4410 + 52,4267
= 107,8677 аму. - Нәтижелерді тексеру үшін периодтық жүйеден сол элементті табыңыз. Орташа куб атомы әрдайым элементтің химиялық белгісінің астында жазылады.
- Орташа атомАг = (куб атомыАг-107 * арақатынасАг-107) + (атомдық массаАг-109 * арақатынасАг-109)
2-ден 2-бөлім: Нәтижелерді пайдалану
Массаны атом санына айналдыру. Орташа масса атомы сол элементтің типтік үлгісіндегі масса мен атомдар саны арасындағы байланысты көрсетеді. Бұл химиялық зертханаларда өте пайдалы, өйткені атомдарды дәл санау мүмкін емес, бірақ массаларын анықтау оңай. Мысалы, сіз күмістің үлгісін өлшеп, әр 107 8677 аму үшін бір күміс атомы болатынын біле аласыз.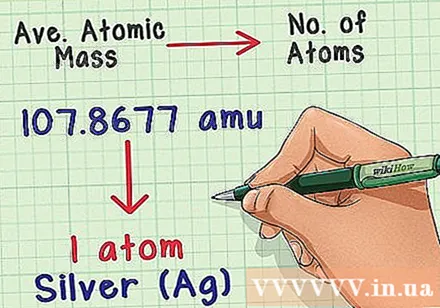
Молярлық массаға айналдыру. Атомдық масса бірлігі өте аз, сондықтан химиктер массаға арналған грамдық бірлікті жиі пайдаланады. Бақытымызға орай, бізде бұл ұғымдардың анықтамалары бар, сондықтан трансформация оңай болуы керек. Нәтижесінде г / моль алу үшін орташа массалық атомды 1 г / мольға (молярлық масса константасы) көбейтіңіз. Мысалы, 107,8677 грамм күмісте бір моль күміс атомы бар.
Орташа молекулалық массаны табыңыз. Молекула атомдардың жиынтығы болғандықтан, молекулалық массаны табу үшін барлық атомдардың массасын қосуға болады. Егер сіз орташа массалық атомды қолданатын болсаңыз (белгілі бір изотоптың массасының орнына), онда нәтиже табиғаттағы үлгінің орташа молекулалық массасы болады. Міне мысал: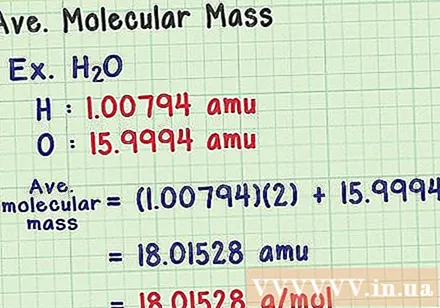
- Су молекуласында H формуласы бар2О құрамында екі сутек атомы (H) және бір оттегі (O) атомы бар.
- Сутектің орташа массалық атомы 100794 аму. Оттегінің орташа атомдық массасы 159994 аму.
- Сонымен Н орташа молекулалық массасы2O (1,00794) (2) + 15,9994 = 18,01528 аму, бұл 18 01528 г / мольге тең.
Кеңес
- Салыстырмалы атомдық масса ұғымы кейде орташа масса атомымен синоним ретінде қолданылады. Шамалы айырмашылық бар, өйткені атомдық масса салыстырмалы түрде бірлікке тең емес; бұл көміртегі-12 атомына қатысты массаны өлшеу. Орташа кубтық атомды есептеу кезінде атомдық масса бірлігін қолданғанша, бұл екі мән бірдей.
- Текше атомынан кейінгі жақшадағы сан бізге қатені айтады. Мысалы, массалық атом 1.0173 (4) элементтің қалыпты атомының массалық ауқымы шамамен 1.0173 ± 0.0004 болатынын білдіреді. Егер бұл сұралмаса, сізге бұл нөмірді алудың қажеті жоқ.
- Периодтық кестеде келесі элементтің орташа куб атомы оның алдындағыға қарағанда үлкен, ерекшеліктері аз. Нәтижелерді тексерудің жылдам әдісі.
- 1 атомдық масса бірлігі - көміртегі-12 атомының 1/12 массасы.
- Изотоптардың тіршілік ету коэффициенттері жер бетіндегі әдеттегі табиғи үлгілерге сәйкес есептеледі. Метеориттер немесе лабораторияда шығарылған табиғи емес заттар изотоптардың әр түрлі қатынасында болуы мүмкін, сондықтан орташа масса атомы да әр түрлі болады.
Ескерту
- Масса атомдары әрдайым атомдық масса бірліктерінде жазылады (аму немесе u), кейде дельтондар (Da) деп аталады. Бұл саннан кейін ешқашан массаның басқа бірлігін (мысалы, килограмм) жазбаңыз, оны өзгертпей.
Сізге не керек
- Қарындаш
- Қағаз
- Ноутбук
- Табиғаттағы изотоптардың өмір сүру деңгейі туралы мәліметтер.
- Изотоптарға арналған жаппай атом бірлігі туралы мәліметтер.